帕米帕利(百汇泽®)说明书(适应症_医保价格_副作用)
发布日期:2021-12-11 浏览次数:

【药品名称】
通用名称:帕米帕利胶囊
商品名称:百汇泽®/PARTRUVIX®
英文名称:Pamiparib Capsules
代号:BGB-290
靶点:PARP-1、PARP-2
【成份】
本品主要成份为帕米帕利。
化学名称:(R)-2-氟-10a-甲基-5,8,9,10,10a,11-六氢-5,6,7a,11-四氮杂环庚三烯并[def]环戊二烯并[a]芴-4(7H)-酮倍半水合物
化学结构式:
分子式:C16H15FN4O·H2O
分子量:325.34
辅料:微晶纤维素微丸丸芯、羟丙甲纤维素、滑石粉和明胶空心胶囊。
【性状】
本品内容物为黄色微丸。
【适应症】
本品适用于既往经过二线及以上化疗的伴有胚系BRCA(gBRCA)突变的复发性晚期卵巢癌、输卵管癌或原发性腹膜癌患者的治疗。
该适应症是基于一项包括113例既往经过二线及以上化疗的伴有gBRCA突变的复发性晚期卵巢癌、输卵管癌或原发性腹膜癌患者中开展的开放性、多中心、单臂、II期临床试验结果给予的附条件批准(参见【临床试验】)。该适应症的完全批准将取决于正在进行的确证性试验证实本品在该人群的临床获益。
【规格】
20 mg(按C16H15FN4O计)。
【用法用量】
本品须在有抗肿瘤治疗经验的医生指导下用药
BRCA突变检测
在使用本品治疗前,应采用国家药品监督管理局批准的检测方法,确定患者存在有害或疑似有害的gBRCA突变,方可使用本品治疗。
推荐剂量
本品推荐剂量为每次60 mg(3粒),每日2次,相当于每日总剂量为120 mg,应持续治疗直至疾病进展或发生不可接受的不良反应。
给药方法
建议患者在每天大致相同时间点口服给药,本品应整粒吞服,不应咀嚼、压碎、溶解或打开胶囊。本品在进餐或空腹时均可服用。
漏服
如果患者发生呕吐或漏服一次药物,不应额外补服,应按计划时间正常服用下一次处方剂量。
剂量调整
针对不良反应的剂量调整
为管理药物不良反应,可根据不良反应的严重程度考虑暂停治疗或减量(见表2和表3)。推荐的剂量调整见表1。

监测全血细胞计数(CBC),建议在治疗的前3个月内每周监测一次,之后定期监测治疗期间出现的具有临床意义的参数变化(见表3)。针对非血液学不良反应的剂量调整

合并使用细胞色素P450(CYP)3A抑制剂
允许合并使用强效/中效/轻效CYP3A抑制剂,无需调整剂量(参见【药物相互作用】)。
特殊人群用药
肾功能不全:
对于轻中度肾功能损害患者,无需调整剂量。尚无本品用于重度肾功能损害患者的研究,重度肾功能损害患者应慎用本品(参见【药代动力学】)。
肝功能不全:
对于轻度肝功能损害患者,无需调整剂量。尚无本品用于中重度肝功能损害患者的研究,中重度肝功能损害患者不推荐使用本品(参见【药代动力学】)。
儿童和青少年:
尚未确立本品在18岁以下患者中的安全性和有效性。
老年人:
对于老年患者(≥65岁),无需调整剂量(参见【老年用药】)。
【不良反应】
本说明书不良反应描述了在临床研究中观察到的判断为可能由帕米帕利引起的不良反应的近似发生率。由于临床研究是在不同条件下进行的,不同临床研究中观察到的不良反应的发生率不能直接比较,也可能不能反映临床实践中的实际发生率。
安全性特征总结
本品的安全性信息来自三项临床试验(BGB-290-102 [患者例数(N)=128]、BGB-290-AU-002 [N=101]和BGB-290-201 [N=88]),共涵盖317例患者。肿瘤类型包括晚期卵巢癌(N=185)、乳腺癌(N=101)、前列腺癌(N=12)、肺癌(N=5)、胶质母细胞瘤(N=3)、软骨肉瘤和胰腺癌(各N=2)以及原发灶不明的腺癌、原发灶不明的癌、宫颈癌、胃癌、平滑肌肉瘤、间皮瘤和子宫癌(各N=1)。上述试验中256例患者接受了60mg/次,每日2次的帕米帕利治疗,61例患者接受了其他剂量的帕米帕利治疗。所有患者(N=317)的中位暴露持续时间为5.5个月(范围:0.1 ~ 57.1个月)。在接受本品治疗的317例患者中,发生率≥10%的不良反应包括:贫血、恶心、白细胞减少症、中性粒细胞减少症、呕吐、疲乏、血小板减少症、食欲减退、腹泻、腹痛、天门冬氨酸氨基转移酶(AST)升高、丙氨酸氨基转移酶(ALT)升高、血胆红素升高以及淋巴细胞减少症。
3级及以上的不良反应发生率为55.8%,发生率≥1%的不良反应包括贫血、中性粒细胞减少症、白细胞减少症、血小板减少症、淋巴细胞减少症、呕吐、疲乏、腹泻、恶心以及AST升高。
与药物相关的严重不良事件(SAE)发生率为21.5%,发生率超过1%的与药物相关的SAE为:贫血和白细胞减少症。
关键性临床试验中的不良反应
BGB-290-102的II期部分是在中国卵巢癌患者中开展的关键性试验,此试验中共有113例患者接受帕米帕利60mg/次,每日2次治疗。中位治疗持续时间为8.3个月(范围:0.1~26.0个月)。
本试验的患者中,发生率≥??10%的不良反应为:贫血、白细胞减少症、恶心、中性粒细胞减少症、呕吐、血小板减少症、食欲减退、疲乏、腹痛、ALT升高、腹泻、AST升高、淋巴细胞减少症、γ-谷氨酰转移酶升高、上呼吸道感染、血胆红素升高、不适、体重降低以及头晕。3级及以上的不良反应发生率为71.7%,其中发生率≥1%的不良反应包括贫血、中性粒细胞减少症、白细胞减少症、血小板减少症、淋巴细胞减少症、呕吐、腹泻、γ-谷氨酰转移酶升高、低钾血症、腹痛、疲乏、上呼吸道感染、全血细胞减少症以及高血压。
导致超过1例患者永久终止帕米帕利治疗的不良反应仅为贫血,其发生率为4.4%。
本试验的患者中,不良反应(发生率≥??5%)汇总见表4,实验室检查异常(发生率≥5%)见表5。
表4: BGB-290-102关键性临床试验中接受帕米帕利治疗的患者中发生率≥??5%的不良反应a
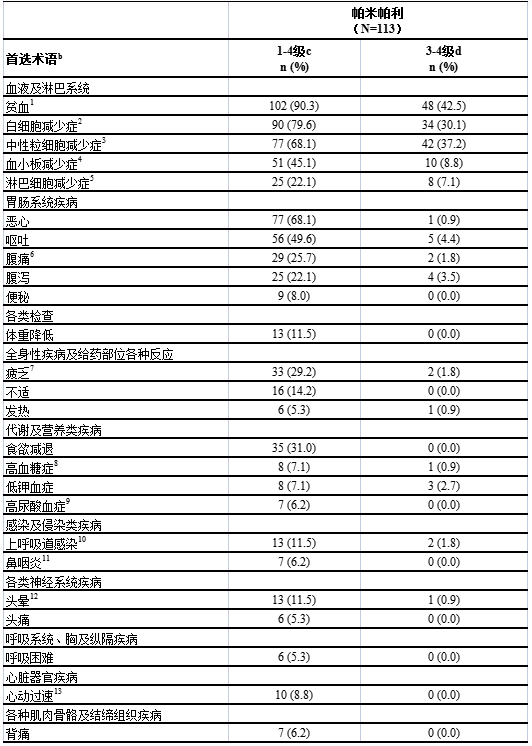
a. 本说明书中的不良反应定义为:研究者判断为与研究药物相关、可能相关、可能无关或无法判断的不良事件,仅除外研究者判断肯定无关的不良事件。数据截止日期为2020年8月24日。
b. 首选术语依据ICH国际医学用语词典(MedDRA)23.0中文版。
c. 不良反应严重程度依据NCI CTCAE v4.03分级。
d. 本研究中无5级不良反应。
以下术语代表描述某种病症的一组相关事件,而不是单一事件。
1. 包括贫血、血红蛋白降低、红细胞减少症、红细胞计数降低。
2. 包括白细胞减少症、白细胞计数降低。
3. 包括中性粒细胞减少症、中性粒细胞计数降低。
4. 包括血小板减少症、血小板计数降低。
5. 包括淋巴细胞减少症、淋巴细胞计数降低。
6. 包括腹胀、腹痛、上腹痛、下腹痛、腹部触痛、上腹不适、腹部不适。
7. 包括疲乏、乏力。
8. 包括高血糖症、血葡萄糖升高。
9. 包括高尿酸血症、血尿酸升高。
10. 包括上呼吸道感染、病毒性上呼吸道感染。
11. 包括鼻咽炎、口咽疼痛、鼻部发炎、鼻塞、鼻充血。
12. 包括头晕、眩晕、体位性头晕。
13. 包括心悸、心动过速、窦性心动过速。
表5: BGB-290-102关键性临床试验中接受帕米帕利治疗的患者中发生率≥??5%的与治疗相关的实验室检查异常a
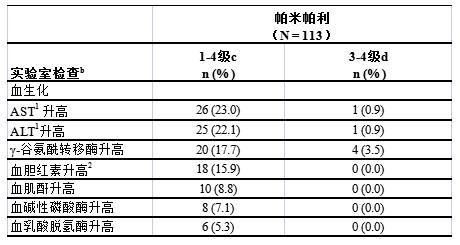
a. 本说明书中的实验室检查异常定义为研究者判断为与研究药物相关、可能相关、可能无关或无法判断的不良事件,仅除外研究者判断肯定无关的不良事件。数据截止日期为2020年8月24日。
b. 实验室检查首选术语依据ICH国际医学用语词典(MedDRA)23.0中文版。
c. 不良反应严重程度依据NCI CTCAE v4.03分级。
d. 本研究中无5级相关实验室异常。
以下术语代表描述某种病症的一组相关事件,而不是单一事件。
1. height="331" referrerpolicy="no-referrer" src="/uploads/allimg/211211/145U52054-5.jpg" style="margin: 0px; padding: 0px; max-width: 100%;" width="410" />
PSOC:对铂类药物敏感的卵巢癌; PROC:对铂类药物耐药的卵巢癌; ORR:客观缓解率; DCR:疾病控制率; CR:完全缓解; PR:部分缓解; SD:疾病稳定; mDoR:中位缓解持续时间; 95% CI:95%置信区间。
在纳入安全性分析集的90例PSOC患者人群中,由IRC评估的中位无进展生存期(mPFS)为15.2个月(95% CI: 10.35, 20.63),中位OS尚未达到;23例PROC患者人群mPFS为6.2个月(95% CI: 4.11, 17.91),中位OS为13.6个月(95% CI: 7.13, 19.75)。
在纳入有效性可评价分析集的82例gBRCA突变的PSOC患者中,75例患者经针对BRCA基因的二代测序(NGS)检测方法确认伴有gBRCA突变,7例患者经针对BRCA基因的多重连接探针扩增技术(MLPA)确认伴有gBRCA突变。在75例NGS检测确认gBRCA突变的患者中,由IRC评估的ORR为69.3%(95% CI: 57.6, 79.5),疾病控制率为94.7%(95% CI: 86.9, 98.5),中位缓解持续时间为13.8个月(95% CI: 9.03, 20.73),中位无进展生存期为15.2个月(95% CI: 10.35, 17.94)。7例MLPA方法确认gBRCA突变的患者中,由IRC评估的ORR为57.1% (4/7,其中1例患者CR,3例患者PR)。
【药理毒理】
药理作用
帕米帕利是一种强效选择性多聚ADP核糖聚合酶(PARP酶,包括PARP1和PARP2)抑制剂,参与DNA修复。体外研究显示,帕米帕利能抑制PARP酶活性以及增加PARP-DNA复合物形成,诱发DNA损伤和癌细胞死亡。帕米帕利可在体外抑制肿瘤细胞的增殖,在小鼠体内抑制人源异种移植肿瘤模型的生长。并且在携带乳腺癌易感基因(BRCA)突变或其他同源重组缺陷(HRD)的肿瘤细胞或小鼠模型中,帕米帕利显示出更强的细胞增殖抑制活性和抗肿瘤作用。
在117例实体瘤患者中采用三联心电图中心读片评估帕米帕利对于心脏复极化的影响。对帕米帕利在不同时间的浓度和QTc相对于基线的变化进行分析,显示本品在60mg/次,每日2次剂量时不会引起临床相关的QTc间期延长。
毒理研究
遗传毒性:帕米帕利体外Ames试验(细菌回复突变)结果为阴性,但中国仓鼠卵巢(CHO)体外细胞染色体畸变试验和体内大鼠骨髓微核试验结果为阳性,可见染色体断裂作用,与帕米帕利药理作用机制一致,提示其在人体中可能具有潜在遗传毒性。
生殖毒性:尚未开展帕米帕利的生育力研究。在剂量高达6mg/kg/天的大鼠3个月重复给药毒性试验和剂量高达3mg/kg/天的犬3个月重复给药毒性试验中,动物生殖器官均未见给药相关的肉眼病变或组织病理学异常。相应剂量下药物暴露量分别相当于人体暴露量(AUC)的0.1和0.02倍。
尚未开展帕米帕利的胚胎/胎仔发育毒性研究。遗传毒性研究显示帕米帕利具有遗传毒性,一般毒理学研究显示帕米帕利具有细胞毒性(骨髓抑制),基于帕米帕利的作用机制,妊娠期间给予帕米帕利具有潜在风险,胎仔暴露于帕米帕利可增加胚胎/胎儿致畸性和/或致死性。
致癌性:尚未开展帕米帕利的致癌性研究。
【药代动力学】
在2.5-120 mg范围内每日两次给药,首次给药后帕米帕利血浆暴露量随剂量成比例增加,稳态时观察到在有限的中国患者中40mg的暴露量与60mg接近。中国患者人群单剂量服用帕米帕利60mg后的几何平均 Cmax 和 AUC0-12 分别是 2275.1 ng/mL 和 16841.5 h*ng/mL。多次给药稳态的Cmax和 AUC0-12 分别是5251.5 ng/mL和 48802.4 h*ng/mL。
吸收
帕米帕利口服给药后吸收迅速,通常在给药后1-2小时达到血浆峰浓度。
摄入高脂早餐后服用帕米帕利60mg吸收延迟,Tmax从2小时延长至7小时。AUC0-inf和Cmax分别降低12%和41%。AUC的降低无临床意义,进餐或空腹状态下均可服用帕米帕利。
分布
帕米帕利的人血浆蛋白结合率为95.7%。60mg 每日两次给药,帕米帕利的表观分布容积大约为37升。
代谢
帕米帕利主要由CYP2C8 和 CYP3A酶代谢。在人体吸收代谢排泄研究中,帕米帕利广泛代谢,药物相关物质主要在尿液中排泄。帕米帕利的主要代谢途径包括氧化(脱氢)反应生成单氧化代谢物、过氧化代谢物,以及氧化葡糖苷酸、水合物和帕米帕利的加成产物。
消除
帕米帕利消除的主要途径为肾脏排泄,平均57.8%的放射性标记给药通过肾脏排泄;次要途径为粪便排泄,放射性标记给药经粪便排泄的回收率均值为26.9%。血浆中消除半衰期t1/2约为13小时。
特殊人群
未对儿童、青少年及不同性别的患者的药代动力学进行研究。
肾功能不全
尚无单独的研究。
在已有临床研究的汇总分析中,通过比较轻度(肌酐清除率CLCR=60-89 mL/min,N=29)和中度(肌酐清除率CLCR=30-59 mL/min,N=10)肾功能受损患者与肾功能正常患者(CLCR≥90 mL/min,N=33)的帕米帕利清除率,来评价肾功能受损对帕米帕利清除率的影响。结果显示,相较肾功能正常患者,轻度肾功能受损患者帕米帕利清除率的几何均值比为0.83,中度肾功能受损患者帕米帕利清除率的几何均值比为1.02。尚无重度肾功能受损患者中帕米帕利清除率的数据。
肝功能不全
尚无单独的研究。
已有临床研究的在汇总分析中,通过比较轻度(总胆红素TB≤正常值上限ULN或TB>ULN且 ≤1.5×ULN,天门冬氨酸氨基转移酶AST>正常值上限ULN,N=19)肝功能受损患者与肝功能正常患者(TB≤ULN,AST≤ULN,N=53)的帕米帕利清除率,来评价肝功能受损对帕米帕利清除率的影响。结果显示,相较肝功能正常患者,轻度肝功能受损患者帕米帕利肌酐清除率几何均值比为0.77。尚无中度(TB>1.5×ULN,≤3.0×ULN)和重度(TB>3.0×ULN)肝功能受损患者中帕米帕利清除率的数据。
【贮藏】
密封,常温保存。
【包装】
高密度聚乙烯瓶及聚丙烯儿童安全组合瓶盖系统:30粒/瓶、60粒/瓶。
高密度聚乙烯瓶及高密度聚乙烯/聚丙烯儿童安全组合瓶盖系统:90粒/瓶。
【价格】
在中国,百汇泽(帕米帕利胶囊)的规格为20mg*60粒,建议零售价为¥7000元/盒.
【有效期】
24个月。
印度肿瘤药房(India Pharmacy)是印度新德里肿瘤药房信息咨询服务平台,旨在为患者提供各类进口原研 进口仿制 最新研制等医药信息咨询 跨境医药电商直邮服务,让患者轻松获取全球最佳药品有更多选择,基本涵盖新特药 抗癌药 靶向药 丙肝 乙肝 高血压 糖尿病 痛风 等药品,欢迎咨询!官方微信 Yindu7689


