- 肿瘤专区
- 肺癌药品
- 色瑞替尼(Ceriti 瑞普替尼,REPODX, 特泊替尼,TEPODX, 克唑替尼,KESODX, 阿来替尼, AILEDX, 普拉替尼,PRASEDX, 奥希替尼(泰瑞沙 阿达格拉西布(Ad 色瑞替尼(赞可达 阿来替尼(安圣莎 阿法替尼(吉泰瑞 Augtyro(repotrectinib, 恩曲替尼(entrec 布格替尼(布加替 布格替尼(布加替 阿达格拉西布(Ad 阿那莫林(Anamorel 塞尔帕替尼 曲美替尼 普拉替尼国内上市 Gavreto普拉替尼( 普拉替尼 索托拉西布(AMG51 奥希替尼|AZD9291 Tagrix80奥希替尼 Crizocent250克唑替尼 Lumakras索托拉西布 吉非替尼Gefitinib( 达拉非尼Dabrafeni Pralsetinib 普拉替尼 Brigatinib 布加替尼 Crizotinib 克唑替尼 Selpercatinib 塞尔帕 Larotrectinib 拉罗替 Savolitinib 沃利替尼 Sotorasib 索托拉西布 Icotinib 埃克替尼 Ceritinib 色瑞替尼, Lorlatinib 劳拉替尼 Capmatinib 卡马替尼 恩曲替尼,entrec Lorbrexen劳拉替尼 Crizonix克唑替尼( 卡马替尼Capmatini 奥希替尼|AZD9291|泰 阿来替尼Alectinib 克唑替尼Crizotini 奥希替尼|AZD9291 布加替尼Briganix 布加替尼 90mg 布加替尼 180mg 吉非替尼|易瑞沙 厄洛替尼|特罗凯 阿法替尼|吉泰瑞 克唑替尼|赛可瑞 阿来替尼|Alecinix 色瑞替尼(SPEXIB) 吉非替尼|易瑞沙 阿法替尼|Afatinib 特罗凯|盐酸厄洛替 克唑替尼|赛可瑞 艾乐替尼|Alecensa 奥希替尼|AZD9291 克唑替尼Crizalk
- 肝癌药品
- 乐伐替尼(仑伐替 乐伐替尼(仑伐替 Donafenib 多纳非尼 培米替尼 培美替尼 培米替尼 培美替尼 印度仑伐替尼/乐伐 Sorafenib索拉非尼( REGONIX瑞格非尼Re 卡博替尼/卡赞替尼 乐伐替尼Lenvanix1 乐伐替尼Lenvanix4 乐伐替尼Lenvaxen1 乐伐替尼Lenvaxen4 乐伐替尼|仑伐替尼 乐伐替尼|仑伐替尼 乐伐替尼|仑伐替尼 卡博替尼 60mg 卡博替尼 20mg 卡博替尼 80mg 索拉非尼|多吉美 索拉非尼|多吉美 索拉非尼|多吉美
- 乳腺癌药品
- 艾拉司群(Elaces 卡帕塞替尼(Cap 阿贝西利(Abemac 瑞博西尼(瑞波西 瑞司美替罗(Rezdi 瑞司美替罗(Rezdi 艾拉司群(elacestr 艾拉司群(elacestr 艾拉司群(elacestr 阿贝西利(Abemac 图卡替尼,TUKADX, 阿贝西利, BESIDX, 图卡替尼(Tucati 阿培利司(Alpeli 新药|Tukysa(Tucatin 氟维司群 芙仕得 芙瑞 来曲唑 Letr 帕捷特 帕妥珠单抗 阿那曲唑,瑞宁得 恩美曲妥珠单抗 西达本胺 爱谱沙 吡咯替尼 艾瑞妮 Enhertu DS8201 100mg( 哌柏西利/帕博西 印度Abemaciclib玻玛 Enhertu(DS-8201)F Palbocent125哌柏西利 印度卡培他滨( 印度版pivikto阿博利 奈拉替尼/来那替尼 印度NATCO拉帕替尼 拉帕替尼Lapatinib 拉帕替尼(泰立沙 Ribociclib 瑞博西尼 Trodelvy 赛妥珠单抗 TUKYSA 图卡替尼 AZD8186 AZD8186 poziotinib 波齐替尼 Lapatinib 拉帕替尼 Trastuzumab 曲妥珠单 Pertuzumab 帕妥珠单 Adavosertib AZD1775 Pyrotinib 吡咯替尼 Alpelisib(阿培利司 哌柏西利|帕博西尼 哌柏西利|帕博西尼 奥拉帕尼Olaparix 来那替尼Hernix 拉帕替尼|泰立沙 哌柏西利|帕博西尼 依维莫司|飞尼妥 哌柏西利|帕博西尼
- 卵巢癌药品
- 尼拉帕尼(Nirapa 奥拉帕尼,OLADX, 奥拉帕尼,OLADX, 奥拉帕利(Olaparib 氟唑帕利 (Fluzopa 百汇泽 帕米帕利 艾瑞颐,氟唑帕利 尼拉帕尼Niranib/( Olaparib 奥拉帕利, Melphalan 马法兰,米 马法兰 爱克兰 美 尼拉帕利 尼拉帕尼 尼拉帕尼Niranib 奥拉帕利Olanib 尼拉帕利Niraparix
- 黑色素癌药品
- 考比替尼(Cobime 康奈非尼,BRATOD 维莫非尼,VEMUDX, 比美替尼-卢修斯 威罗非尼(佐博伏 达拉非尼(Tafinl Dabrafenib 达拉非尼 Mektovi(Binimetinib)贝 特瑞普利单抗 拓益 Vismodegib维莫德 Yervoy伊匹单抗(I (BRAF V600E/K突变组 司美替尼Koselugo( 威罗菲尼(Zelbor Cotellic土耳其Cobi 替莫唑胺Temonix 曲美替尼Trametini 替莫唑胺GLIOZ 替莫唑胺|蒂清 达拉非尼Dabrafeni
- 肝病专区
- 肺癌专区
- 肺癌药品
- 兰泽替尼片(Luc 达拉非尼,DABRAD 卡马替尼,CAMPAM 索托拉西布,SOT 劳拉替尼,LORLAD 曲美替尼,TRAMED 莫博替尼, MOBODX, 奥西替尼, OYSIEND 卡博替尼,CABODX, 卡博替尼,CABODX, 卡博替尼,CABODX, 塞尔帕替尼,SEP 恩曲替尼,ENTRED 拉罗替尼, LARODX, 拉罗替尼,LARODX,L 比美替尼,MEKTODK, 特泊替尼Tepotinib 索托拉西布Lumakr Adlumiz阿那莫林说明 阿来替尼(安圣莎 赛沃替尼片(沃瑞 奥希替尼/奥西替尼 普拉替尼 (Pralset Trametinib 曲美替尼 Lumakras Tablets 240× 塞尔帕替尼Selper Selpercatinib 塞尔帕 Anlotinib 安罗替尼 替雷利珠单抗、百 普拉替尼,普吉华 赛沃替尼 Savoliti 艾弗沙、伏美替尼 阿美替尼,阿美乐 卡瑞利珠单抗 艾瑞 sumab(Xgeva) 地诺 恩沙替尼 (Ensarti 达拉非尼Dabrafeni 曲美替尼 迈吉宁 劳拉替尼Lorviqua Brigatinib布吉替尼 纳武利尤单抗/40 纳武利尤单抗/10 afatinib阿法替尼(吉 Osicent80奥希替尼 Osimert奥希替尼Os Dacocare达克替尼(
- 肾癌专区
- 胃直肠癌
- 骨髓血癌
- 白血病药品
- 奎扎替尼(Quizar 奎扎替尼(Quizar 阿西米尼(Ascimi 达沙替尼 20mg说明 吉瑞替尼,GILLID 维奈托克,VECLAD 恩西地平,ENASID 艾伏尼布, AIVODX, quizartinib,奎扎替 奎扎替尼quizartin 帕纳替尼(Ponatini 帕纳替尼(Ponatini 维奈克拉片(ven 普纳替尼(Ponati 阿西米尼(ascimi 阿西米尼/阿西米尼 阿扎胞苷片(Aza 艾伏尼布 吉列替尼 吉瑞替尼 阿伐曲泊帕(Ava 艾曲波帕(Revola Celrixafor释倍灵/普 Venetoclax 维奈托克 Ponaxen45普纳替尼 达沙替尼Dasatinib( 伊马替尼Gleevec,i 帕纳替尼Ponatinib 普纳替尼Ponatinix 伊马替尼|格列卫 达沙替尼 20mg 达沙替尼 50mg 达沙替尼 100mg 达沙替尼|施达赛 格列卫|伊马替尼片 格列卫|伊马替尼
- 新特药区
- 风湿骨病药品
- 非戈替尼(Filgot 非戈替尼(Filgot 托法替尼,TOFADX, 乌帕替尼,UPADX, 巴瑞替尼, BARUDX, 巴瑞替尼, BARUDX, 莫洛替尼momelotin 非戈替尼 乌帕替尼(upadac 乌帕替尼(upadacit 托法替布(5mg*60) 托法替尼(Tofaci 巴瑞克替尼、巴瑞 非布司他(优立通 非布司他 ZURIG 托法替尼Tocit 托法替尼Tofanib 托法替尼Tofacinix 非布司他 ZURIG80 托法替布Tofacitin 巴瑞克替尼 4mg 巴瑞克替尼 2mg
- 糖尿病药品
- 曲格列汀(Zafate 曲格列汀,TEGLID 非奈利酮(finereno 口服司美格鲁肽( 口服司美格鲁肽( 口服司美格鲁肽( Eudaxen(Diazoxide)二氮 恩格列净(欧唐静 琥珀酸曲格列汀( 恩格列净(欧唐静 曲格列汀(Zafatek) 曲格列汀片 50mg 曲格列汀片 100mg
- 特效药
- 阿普昔腾坦(Apr 达普司他(Daprod 维贝格龙(Vibegr 贝舒地尔(Berdaz 西多福韦(Cidofo 芦曲泊帕,LUTROD 阿那格雷(Anagreli 万赛维(盐酸缬更 艾曲波帕,ELTROM 艾曲波帕,ELTROM 阿伐曲波帕, AVAT 甲磺酸贝舒地尔片 非达霉素 醋酸环丙孕酮片( 斯佩格(SPEGRA) 印度迈兰Mylan三合 达可辉的作用与功 司帕生坦(sparse 泰毕全(达比加群 Rutinib-5(Ruxolitinib Tafero/EM达可挥( TAFFIC(必妥维)塔菲 Myltega特威凯(DTG)多 spegra斯佩格| 三合 奥贝胆酸Obetix
- 其他药品


万赛维(盐酸缬更昔洛韦片)是更昔洛韦(ganciclovir)的前体药物,是一种活性更昔洛韦缬氨酸酯。它口服后可在肠道和肝脏细胞中被磷酸酯酶迅速水解成更昔洛韦,发挥抗病毒作用。
药品称呼
通用名称:Valganciclovir
商品名称:VALCYTE
英文名称:Valganciclovir
中文名称:盐酸缬更昔洛韦片
全部名称:万赛维、盐酸缬更昔洛韦片、VALCYTE、Valganciclovir
剂型和规格
1、VALCYTE片剂:450毫克、粉红色、薄膜包衣凸形椭圆形片剂,一面上刻有“VGC”,另一面刻有“450”。
2、VALCYTE口服溶液:50毫克/毫升,供应时为白色至微黄色粉末,配制后形成无色至棕黄色的什锦水果口味调味溶液。采用玻璃瓶包装,配制后可提供约100毫升溶液。
特殊人群用药
1、妊娠期
口服给药后,缬更昔洛韦(前药)转化为更昔洛韦(活性药物),因此,预计VALCYTE具有与更昔洛韦相似的生殖毒性作用。在动物研究中,更昔洛韦对怀孕小鼠和家兔造成母胎毒性和胚胎-胎儿死亡率,对家兔的致畸性是人类暴露量的两倍。尚无关于孕妇使用VALCYTE或更昔洛韦以确定是否存在药物相关风险的可用人体数据。这些人群发生重大出生缺陷和流产的背景风险尚不清楚。
体内外人体胎盘模型的数据显示,更昔洛韦可穿过人体胎盘。这种转移是通过被动扩散进行的,在1至10毫克/毫升的浓度范围内没有饱和转移。
2、哺乳期
目前尚无有关缬更昔洛韦(前药)或更昔洛韦(活性药物)在人乳中的存在、对母乳喂养婴儿的影响或对乳汁分泌的影响的数据。动物实验数据表明,更昔洛韦会从哺乳期大鼠的乳汁中排出。美国疾病控制和预防中心建议感染艾滋病毒的母亲不要用母乳喂养婴儿,以避免产后传播艾滋病毒的风险。建议哺乳期母亲在使用 VALCYTE 治疗期间不建议进行母乳喂养,因为哺乳期婴儿可能会出现严重不良事件,而且可能会传播 HIV。
3、具有生殖潜力的男性和女性
具有生育能力的女性在开始使用VALCYTE前应接受妊娠检测。
避孕:
1)女性
由于VALCYTE具有诱变和致畸潜能,因此应建议具有生育能力的女性在治疗期间和使用VALCYTE治疗后至少30天内采取有效的避孕措施。
2)男性
由于VALCYTE具有诱变潜力,建议男性在使用VALCYTE治疗期间和治疗后至少90天内使用避孕套。
不孕症:
VALCYTE 的推荐剂量可能会导致暂时性或永久性的女性和男性不孕症。
4、儿童使用
VALCYTE口服溶液和片剂适用于预防4个月至16岁的小儿肾移植患者和1个月至16岁有患CMV疾病风险的小儿心脏移植患者的CMV疾病。
在4个月至16岁的儿科肾移植患者中使用VALCYTE口服溶液和片剂预防CMV疾病是基于两项针对4个月至16岁患者的单臂、开放标签、非比较性研究。研究1是对小儿实体器官移植患者(肾脏、肝脏、心脏和肾脏/胰脏)进行的安全性和药代动力学研究。VALCYTE在移植后10天内每日给药一次,移植后最长给药100天。研究2是一项安全性和耐受性研究,在小儿肾移植患者中,VALCYTE在移植后10天内每天给药一次,最长时间为移植后200天。 这些研究的结果得到了先前在成人患者中进行的疗效展示的支持。
将VALCYTE口服溶液和片剂用于预防1个月至16岁小儿心脏移植患者的CMV疾病是基于两项研究(上述研究1和研究3),并得到了先前在成人患者中的疗效证明 。研究3是一项 VALCYTE 的药代动力学和安全性研究,研究对象是年龄小于 4 个月的小儿心脏移植患者,这些患者连续两天各接受一次 VALCYTE 口服液。根据现有的儿科和成人患者的药代动力学数据,我们建立了一个基于生理学的药代动力学(PBPK)模型,以支持年龄小于 1 个月的心脏移植患者的用药。然而,由于新生儿模型预测的不确定性,VALCYTE 不适用于该年龄组的预防。
VALCYTE口服溶液和片剂在儿童中预防 CMV 疾病的安全性和有效性尚未得到确定,包括小儿肝移植患者、小于 4 个月的肾移植患者、小于 1 个月的心脏移植患者、患有 CMV 视网膜炎的小儿艾滋病患者以及患有先天性 CMV 感染的婴儿。
5、老年用药
尚未对 65 岁以上的成人进行 VALCYTE 口服液或片剂的研究。VALCYTE 的临床研究未包括足够数量的 65 岁及以上受试者,因此无法确定他们的反应是否与年轻受试者不同。一般而言,老年患者的剂量选择应谨慎,通常应从剂量范围的低端开始,这反映了肝功能、肾功能或心功能下降以及伴随疾病或其他药物治疗的频率较高。众所周知,VALCYTE 会通过肾脏大量排泄,因此肾功能受损的患者发生毒性反应的风险可能更高。由于肾脏清除率随年龄增长而降低,因此在给药 VALCYTE 时应考虑患者的肾脏状况。应监测肾功能并相应调整剂量。
6、肾功能损害
肾功能损害患者接受VALCYTE给药时,建议减少剂量。
对于接受血液透析(CrCl 低于10毫升/分钟)的成人患者,不应使用 VALCYTE 片剂。成人血液透析患者应按照剂量减少算法使用更昔洛韦。
7、肝功能损害
尚未对肝功能受损患者服用 VALCYTE 的安全性和有效性进行研究。
禁忌症
对缬更昔洛韦、更昔洛韦或制剂的任何组分有临床意义的超敏反应(如过敏反应)的患者禁用。
药物相互作用
尚未使用缬更昔洛韦进行体内药物相互作用研究。然而,由于缬更昔洛韦会迅速且广泛地转化为更昔洛韦,预计缬更昔洛韦会出现与更昔洛韦相关的药物间相互作用。在肾功能正常的患者中进行了更昔洛韦的药物间相互作用研究。VALCYTE和其他经肾脏排泄的药物联合给药后,肾功能受损患者可能会出现更昔洛韦和联合给药药物浓度升高的情况。因此,应密切监测这些患者更昔洛韦和联合用药的毒性。
下表列出了更昔洛韦与已确定的和其他潜在的显著药物相互作用。
表:更昔洛韦已确定的和其他潜在的显著药物相互作用
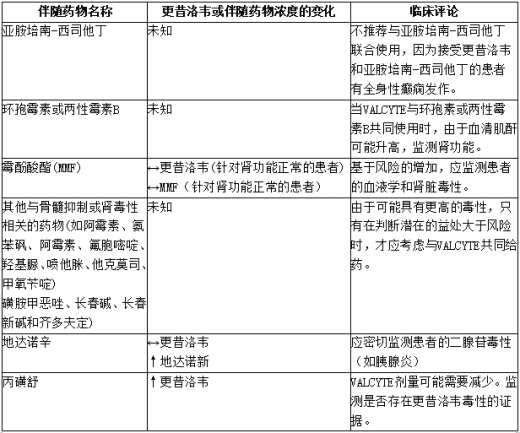
药物过量
使用 VALCYTE 片剂的经验:过量服用 VALCYTE 可能会导致肾毒性增加。由于更昔洛韦可透析,透析可能有助于降低过量服用 VALCYTE 患者的血清浓度。应保持足够的水分。应考虑使用造血生长因子。
从临床试验和上市后经验中收到了关于过量使用缬更昔洛韦后出现不良反应的报告,其中一些不良反应导致死亡。大多数患者都出现了以下一种或多种不良反应:
血液毒性:骨髓抑制,包括全血细胞减少、骨髓衰竭、白细胞减少、中性粒细胞减少、粒细胞减少
肝毒性:肝炎,肝功能异常
肾毒性:既往有肾功能损害、急性肾损伤、肌酐升高的患者血尿恶化
胃肠道毒性:腹痛、腹泻、呕吐
神经毒性:全身性震颤、癫痫
成分
有效成分:Valganciclovir(盐酸缬更昔洛韦)
片剂的非活性成分:微晶纤维素、聚维酮 K-30、氯丙维酮和硬脂酸。片剂的薄膜涂层含有Opadry Pink。
口服溶液的非活性成分:苯甲酸钠、富马酸、聚维酮K-30、糖精钠、甘露醇和什锦水果口味调味料。
性状
片剂、口服液
贮存方法
1、将VALCYTE片剂储存在20°C至25°C的室温下。
2、将VALCYTE口服液在2°C至8°C的冰箱中储存不超过49天。
3、不要冷冻。
4、不要保存过期或不再需要的VALCYTE。
5、将VALCYTE和所有药物放在儿童拿不到的地方。
印度肿瘤药房(India Pharmacy)是印度新德里肿瘤药房信息咨询服务平台,旨在为患者提供各类进口原研 进口仿制 最新研制等医药信息咨询 跨境医药电商直邮服务,让患者轻松获取全球最佳药品有更多选择,基本涵盖新特药 抗癌药 靶向药 丙肝 乙肝 高血压 糖尿病 痛风 等药品,欢迎咨询!官方微信 yindu948


![[field:title /]](/style/images/star.png)




