那些治疗HL的国产PD-1(派安普利单抗卡瑞利珠单抗,信迪利单抗,替雷利珠单抗)
发布日期:2021-12-04 浏览次数:
关于“治疗HL的国产PD-1(派安普利单抗卡瑞利珠单抗,信迪利单抗,替雷利珠单抗)”的相关内容,相信很多病友都想知道,为了方便大家了解,觅健小编搜集整理了有关“治疗HL的国产PD-1(派安普利单抗卡瑞利珠单抗,信迪利单抗,替雷利珠单抗)”的一些资料分享给大家,希望能帮助到大家,供参考。
2021年8月5日,国家药监局最新药品批件发布信息,康方生物/正大天晴共同开发的PD-1单抗药物派安普利单抗已获国家药监局批准上市,用于治疗至少经过二线系统化疗复发或难治性经典型霍奇金淋巴瘤(r/r cHL)患者。

本次获批派安普利单抗是国内上市的第7款PD-1单抗药物,也是第5款国产PD-1。值得注意的是,这次派安普利获批的适应症与先前获批的3款国产PD-1一样,都是r/r cHL。
PD-1与r/r cHL的不解之缘
大约10年前,乔·康纳斯在著名国际医学期刊新英格兰医学杂志发表的一篇文章中,恰如其分地将霍奇金淋巴瘤(HL)确定为肿瘤学的"伟大老师"[1]。之所以赋予HL这一头衔,是因为几代肿瘤学研修者都是通过在HL中倾注了数十个随机试验来学习他们的临床研究课。
如今,10年过去了,这句话里所描述的事情似乎正在我国国产PD-1的研发上市领域重演着。算上刚刚获批的派安利普单抗,目前国家药品监督管理局(NMPA)总共批准了7种PD-1抗体药物上市,其中包含5款国产PD-1。在这5款国产PD-1中,除特瑞普利单抗(Toripalimab)的适应症为晚期黑色素瘤的治疗以外,其余4款PD-1的获批均是从治疗HL开始的。另外两款进口药——帕博利珠单抗和纳武利尤单抗,尽管在国内治疗HL的适应症没有获批,但其已经在包括欧美的多个国家获批用于HL的治疗,甚至被纳入指南[2]。
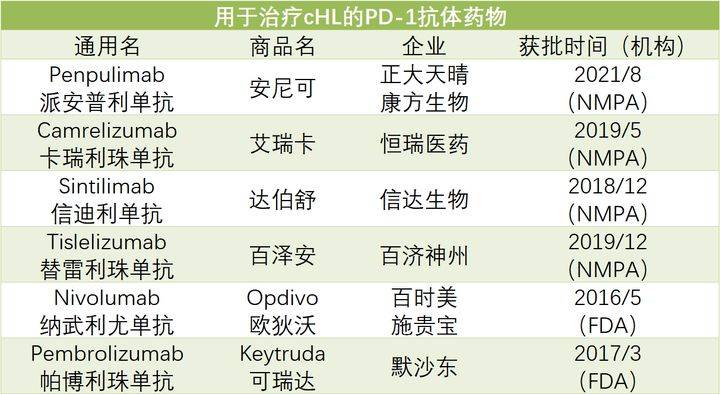
此次派安普利的获批,让以r/r cHL为适应症的PD-1家族更加壮大。那么,这些国产PD-1的效果和安全性究竟如何呢?下面我们就一起来盘点一下派安利普和它的国产PD-1“前辈”们吧~
盘点:那些治疗HL的国产PD-1
派安普利单抗
新晋国产PD-1派安普利单抗,由康方生物/正大天晴共同开发,用于治疗至少经过二线系统化疗复发或难治性经典型霍奇金淋巴瘤(r/r cHL)患者。
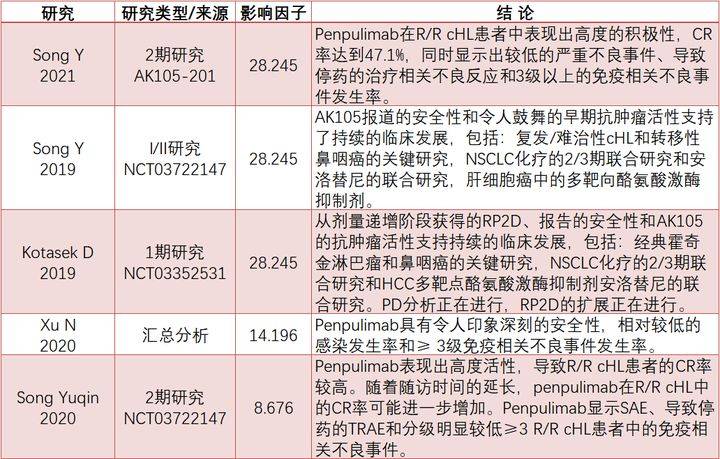
此次派安普利的获批是基于一项多中心、单臂、开放标签的关键性临床试验。研究结果显示:派安普利的客观缓解率(ORR)为89.4%,其中有47.1%的患者达到完全缓解(CR)。中位随访时间为15.8个月,中位缓解持续时间(DoR)未达到,12个月的DoR率为74.9%。中位无进展生存期(PFS)未达到,12个月的PFS率为72.1%。
在安全性方面,派安普利单抗的中位暴露时间为14.8个月,76.6%的患者使用派安普利单抗治疗12个月或以上。与派安普利单抗相关的严重不良事件(SAE)发生率为10.6%,未发生超过1例患者的与药物相关的SAE。3级及以上的不良反应发生率为26.6%,常见药物相关不良反应(≥2%)包括皮疹、高脂血症和肺部感染。3级免疫相关不良事件(irAEs)的发生率为4.3%,未发生三级以上的irAEs。
卡瑞利珠单抗
卡瑞利珠单抗由恒瑞医药自主研发,2019年5月获得NMPA附条件批准上市,适应症为:用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤(R/R cHL)患者的治疗。
在支持卡瑞利珠单抗获批治疗cHL的2期临床试验中,平均随访12.9个月,76.0%的患者客观有效,分别包括28.0%的完全缓解(CR)和48.0%的部分缓解(PR)患者。最常见的不良反应是皮肤反应性毛细血管内皮增生(97.3%)和发热(42.7%)。3级或4级治疗相关不良事件占26.7%;最常见的是白细胞计数下降(4.0%)。无5级治疗相关不良事件[5]。
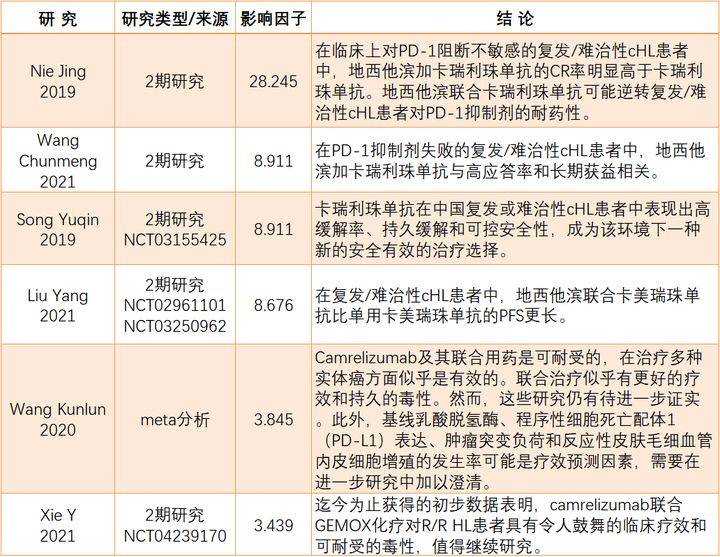
另有研究表明,卡瑞利珠单抗联合地西他滨治疗cHL6个月时的持续反应率为100%。对于先前接受抗PD-1治疗的患者,在地西他滨加卡美瑞珠单抗治疗后,28%的患者获得完全缓解,24%的患者获得部分缓解。10名患者在6个月以上仍有应答,81%的应答者估计在1年以上有应答。[3]而卡瑞利珠单抗联合吉西他滨和奥沙利铂(GEMOX)在治疗cHL方面也具有令人鼓舞的疗效和安全性[8]。
信迪利单抗
信达生物的PD-1抗体药物信迪利单抗是国内首批PD-1抗体药物,在2018年12月被NMPA批准上市,用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的治疗。
在国内最大的cHL队列研究ORIENT-1的2期临床试验中,信迪利单抗的客观缓解率(ORR)达到了74%,有24%的患者完全缓解。最常见的常见的治疗相关不良事件(TRAE)是发热(43.8%),其中92.9%为1~2级。大多数发热发生在输液当天,并在1天内恢复。其他常见的TRAE是甲状腺功能减退(13.5%)和促甲状腺激素升高(11.5%),均为1~2级。最常见的3~4级TRAE是发热(3.1%)和血小板减少(2.1%)[10]在随后的ORIENT-1延长随访中,ORR达到85.4%,完全缓解率29.2%。最常见的TRAE为发热(40.6%),其中92.3%为1级或2级。最常见的3级或4级TRAE为发热(3.1%)和贫血(3.1%)[9]。
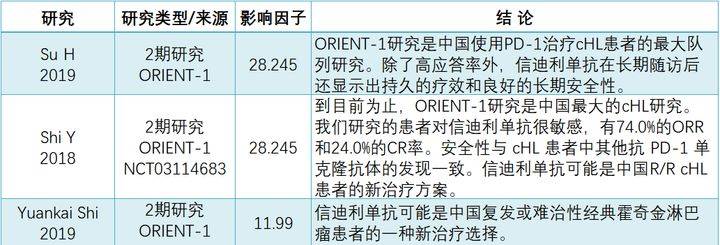
总体来说,信迪利单抗在长期随访后显示出了良好的疗效和安全性,可以成为治疗R/R cHL的一种新的选择。
替雷利珠单抗
替雷利珠单抗是百济神州自主研发的一款PD-1单抗药物,2019年12月被NMPA批准用于治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤患者。
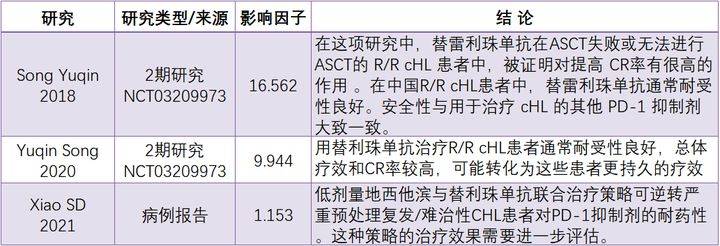
在支持替雷利珠单抗获批治疗cHL的临床2期研究中,87.1%的患者客观缓解,62.9%的患者完全缓解。最常见的不良事件为上呼吸道感染和肺炎,38.6%的患者出现输液相关反应,38.6%的患者出现免疫相关不良事件,其中最常见的是甲状腺功能不全[13]。使用替雷利珠单抗治疗R/R cHL总体疗效较高且耐受性良好,但相关临床数据较少,还需要更多数据支持。
就目前获得的临床数据来看,国产PD-1抗体药物在治疗R/R cHL方面,具有良好的疗效和安全性,甚至优于纳武利尤单抗和帕博利珠单抗。但是与进口PD-1相比,国产PD-1相关临床研究较少,所获批准一般是为满足临床需求进行的有条件批准,其临床试验结果尚不稳健,需要更多的确切的临床数据给予进一步支持。
在价格方面,早前获批的三款国产PD-1的年治疗费用在几万到十几万不等。所幸这三款药均已纳入医保,报销后年治疗费用约1~3万,对于有医保的患者,可以大大降低治疗负担。
国产PD-1未来可期
如今,国产PD-1的研发上市已成红海,先发者占据了有利赛道,留给后来者的机会越来越少,此次派安普利单抗能在激烈的竞争中成功获得一席之地实属不易。

不过,国产PD-1的“内卷”,对于癌症患者来说却不失为一件好事。一方面,竞争的压力可以促使药企积极开发疗效和安全性更好的药物,有利于国产药品质的提升。另一方面,对于有限的市场,价格战的打响在所难免,进而能够促使药价的下降。或许有一天,即使没有医保,PD-1的价格也不再那么“高不可攀”,变成买得到用得起的良药。
参考文献:
[1]Connors JM. Hodgkin’s lymphoma: the great teacher. N EnglJ Med. 2011;365(3):264-265.
[2]Sattva S Neelapu,Sherry Adkins,Stephen M Ansell,etal. Society for Immunotherapy of Cancer (SITC) clinical practice guidelineon immunotherapy for the treatment of lymphoma.J Immunother Cancer,2020,8(2).
[3]Nie Jing,Wang Chunmeng,Liu Yang,et al. Addition of Low-Dose Decitabine toAnti-PD-1 Antibody Camrelizumab in Relapsed/Refractory Classical HodgkinLymphoma[J]Journal of clinical oncology, 2019.
[4]Wang Chunmeng,Liu Yang,Dong Liang,et al. Efficacy of Decitabine plus Anti-PD-1Camrelizumab in Patients with Hodgkin Lymphoma Who Progressed or Relapsed afterPD-1 Blockade Monotherapy[J]Clinical cancer research, 2021.
[5]Song Yuqin,Wu Jianqiu,Chen Xinchuan,,et al. A Single-Arm, Multicenter, Phase IIStudy of Camrelizumab in Relapsed or Refractory Classical HodgkinLymphoma[J]Clinical cancer research, 2019.
[6]Liu Yang,Wang Chunmeng,Li Xiang,et al. Improved clinical outcome in arandomized phase II study of anti-PD-1 camrelizumab plus decitabine inrelapsed/refractory Hodgkin lymphoma[J]Journal for immunotherapy of cancer,2021.
[7]Wang Kunlun,Li Bingxu,et al. The Safety and Efficacy of Camrelizumab and ItsCombination With Apatinib in Various Solid Cancers[J]Frontiers in Pharmacology,2020.
[8]Xie Y,Mi L,Zheng W,et al. Camrelizumab combined with gemox in patients withrelapsed or refractory Hodgkin lymphoma[J]Hematological Oncology, 2021.
[9]Su H,Song Y,Jiang W,et al. Sintilimab for relapsed/refractory classicalHodgkin's lymphoma: Extended follow-up on the multicenter, single-arm phase IIORIENT-1 study[J]Journal of Clinical Oncology, 2019.
[10]Shi Y,Su H,Song Y,Jiang W,et al. Sintilimab (IBI308) in relapsed/refractoryclassical Hodgkin lymphoma: A multicenter, single-arm phase 2 trial in China(ORIENT-1 study)[J]Journal of Clinical Oncology, 2018.
[11]Yuankai Shi,Hang Su,Yongping Song,et al. Safety and activity of sintilimab inpatients with relapsed or refractory classical Hodgkin lymphoma (ORIENT-1): amulticentre, single-arm, phase 2 trial[J]The Lancet Haematology, 2019.
[12]Song Yuqin,Gao Quanli,Zhang Huilai,et al. Tislelizumab (BGB-A317) forRelapsed/Refractory Classical Hodgkin Lymphoma: Preliminary Efficacy and SafetyResults from a Phase 2 Study[J]Blood, 2018.
[13]Yuqin Song,Quanli Gao,Huilai Zhang,et al. Treatment of relapsed or refractoryclassical Hodgkin lymphoma with the anti-PD-1, tislelizumab: results of a phase2, single-arm, multicenter study[J]Leukemia, 2020.
[14]Xiao-Sheng Ding,Lan Mi,et al. Relapsed/refractory classical Hodgkin lymphomaeffectively treated with low-dose decitabine plus tislelizumab:A case report[J]WorldJournal of Clinical Cases, 2021.
[15]Song Y,Zhou K,Jin C,Qian Z,et al. A phase II study of penpulimab, an anti-PD-1antibody, in patients with relapsed or refractoryclassic Hodgkin lymphoma(cHL)[J]Journal of Clinical Oncology, 2021.
[16]Song Y,Zhu J,Lin N,Zhang C,et al. A phase I/II study of the anti-programmedcell death-1 (PD-1) antibody AK105 in patients with relapsed or refractoryclassic Hodgkin lymphoma (cHL)[J]Journal of Clinical Oncology, 2019.
[17]Kotasek D,Coward J,De Souza P L,et al. A phase I dose escalation and doseexpansion study of the anti-programmed cell death-1 (PD-1) antibodyAK105[J]Journal of Clinical Oncology, 2019.
[18]Xu N,Han B,Jiao S,Hu C,et al. 31P Integrated safety analysis of anti-programmedcell death-1 (PD-1) antibody penpulimab in advanced solid tumour orlymphoma[J]Annals of Oncology, 2020.
[19]Song Yuqin,Zhou Keshu,Jin Chuan,et al. 791 A phase II study of the anti-programmedcell death-1 (PD-1) antibody penpulimab in patients with relapsed or refractoryclassic hodgkin lymphoma (cHL)[J]Journal for ImmunoTherapy of Cancer, 2021.
印度肿瘤药房(India Pharmacy)是印度新德里肿瘤药房信息咨询服务平台,旨在为患者提供各类进口原研 进口仿制 最新研制等医药信息咨询 跨境医药电商直邮服务,让患者轻松获取全球最佳药品有更多选择,基本涵盖新特药 抗癌药 靶向药 丙肝 乙肝 高血压 糖尿病 痛风 等药品,欢迎咨询!官方微信 Yindu7689


